
主な合併症治療,対策,管理
1.不整脈
1)洞結節機能不全
2)上室性頻拍(回帰性,自動能亢進)
ペースメーカ植込み
①薬物
ジゴシン,アスペノン,β遮断薬, ソタロール,アンカロン,等
②カテーテルアブレーション
③ 手術(Maze,TCPC転換術等)
2.蛋白漏出性腸症
1)感染(炎症)の有無
2)血行動態評価
Fontanルート狭窄
肺静脈狭窄
体肺側副血行路の有無
心室機能低下
房室弁機能不全
3)過剰水分
感染治療
血行動態改善
カテ治療,手術
コイル塞栓
心不全療法
血管拡張薬,手術
水分管理,利尿薬
3.肺動静脈瘻
1)血行動態評価
肝静脈血流の不均等
酸素投与,肺血管拡張薬
Fontanルート転換
4.血栓症
1)発生部位診断(CT) 血栓溶解術,血栓除去術
5.房室弁閉鎖不全 中等度以上抗心不全療法,手術
6.喀血 1)発生部位診断(CT) 止血剤,コイル塞栓
1.不整脈
1)洞結節機能不全
2)上室性頻拍(回帰性,自動能亢進)
ペースメーカ植込み
①薬物
ジゴシン,アスペノン,β遮断薬, ソタロール,アンカロン,等
②カテーテルアブレーション
③ 手術(Maze,TCPC転換術等)
2.蛋白漏出性腸症
1)感染(炎症)の有無
2)血行動態評価
Fontanルート狭窄
肺静脈狭窄
体肺側副血行路の有無
心室機能低下
房室弁機能不全
3)過剰水分
感染治療
血行動態改善
カテ治療,手術
コイル塞栓
心不全療法
血管拡張薬,手術
水分管理,利尿薬
3.肺動静脈瘻
1)血行動態評価
肝静脈血流の不均等
酸素投与,肺血管拡張薬
Fontanルート転換
4.血栓症
1)発生部位診断(CT) 血栓溶解術,血栓除去術
5.房室弁閉鎖不全 中等度以上抗心不全療法,手術
6.喀血 1)発生部位診断(CT) 止血剤,コイル塞栓
5 治療・管理
術後遠隔期合併症に対する内科的治療,ペースメーカ装着,CRT等の侵襲的治療,そして,右房- 肺動脈の直接吻合(APC型) 法からTCPC型の修
復に変更するFontan Conversion法までを含む.
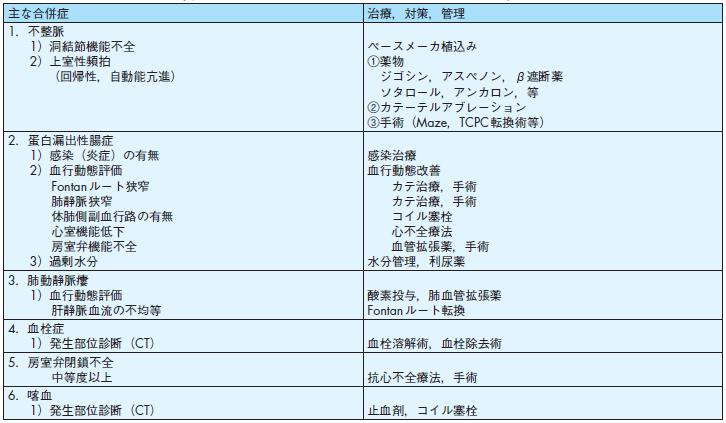
術後遠隔期合併症の治療と管理(表83).特異なFontan循環に由来する合併症が多く,最優先事項はFontan循環の正確な把握にある.必要に応じ
て心臓カテーテル検査を含めた血行動態の把握が必要で,血行動態の改善が合併症管理と治療効果改善に欠かせない.
①不整脈
リエントリーを機序とする心房内リエントリー性頻拍(IART; intra atrial reentrant tachycardia)と自動能亢進による異所性心房頻拍(EAT; ectopic
atrial tachycardia)が多く,時に致死的である.TCPCがAPCに比べ発症頻度が少ないとされるが,TCPCの術式間での発症頻度の差は明確でない
44).術式に関係なく経年的に増加するとされ1050),1051),特に心房臓器錯位症候群で多い1051).徐脈性不整脈もまれでなく,特に左相同型の心房臓器
錯位症候群で多く,ペースメーカ植込みの適応例も少なくない1052).
治療:心房内リエントリー性頻拍や異所性心房頻拍はカテーテルアブレーションは有効だが,約半数で再発する384).したがって,β遮断薬,治療抵抗
性の場合にはソタロールやアミオダロンを考慮する必要があり,一定の効果が期待できる.これらⅢ群薬使用時は,ソタロールではQT延長等の催不整
脈作用,アミオダロンでは肝,甲状腺や肺機能障害発症に充分注意しながらの投与が必要である.APCでのこれら不整脈合併の場合にはTCPC転換
術を行うことがあるが1053),周術期に手術侵襲にも関連した頻拍性不整脈発症の頻度は高い.TCPC転換術を行う際にはペースメーカによる最低心拍
数維持等の心拍数調節を考慮した不整脈管理が重要である.
②蛋白漏出性腸症(PLE; protein losing enteropathy)
術後遠隔期の4 ~ 13%に発症するとされ,経年的に増加し,術後10および20年での発症回避率は92および86%とされる1054).一旦発症した場合の
予後は極めて不良とされ発症後5および10年の死亡回避率は約50および80%である1054).最近の肺血管拡張薬の進歩による予後改善の有無は不明
である.高い静脈圧と関連し,感染が引き金になることが多いとされる1055).モデル実験結果からも,これらがPLE増悪因子であることは疑いない1056).
また,発症時は不整脈(約30%)や血栓症(約20%)等,他の合併症を併発していることも少なくない1054).
治療は感染に関連した炎症の有無を確認,対処する.不整脈治療を含めた心血行動態の最適化と改善余地を模索し,心拍出量を維持した中心静脈
圧(CVP)低下を目指す.中心静脈圧を下げるべく,水分過剰には水分制限・利尿剤,Fontan経路狭窄・肺静脈狭窄にはカテーテル治療あるいは手術
治療,体肺側副血行路による左右短絡にはコイル塞栓術,心室機能低下例では薬物治療,房室弁機能不全手術適応の有無を確認する必要がある.
さらに肺血管抵抗軽減を期待した酸素投与,肺血管拡張薬を考慮する.炎症関連病態にパルス療法を含めたステロイド療法が有効である可能性があ
る1057).Fontanルートと機能的左房との開窓をカテーテルあるいは手術で行うと中心静脈圧降下と心拍出量増加に有効な場合がある1058).初期の多
施設研究では,いずれの治療も一定の有効性はあるが全体の44%しか改善しなかった1054).小児ではヘパリン療法(皮下注)でその症状は76%で改
善するが予後改善の有無は不明で,再入院やアルブミン投与頻度はヘパリン投与前後で変化がないとされる1059).ヘパリン療法の成人Fontan術後患
者での有効例も報告されている1060).肺血管拡張薬(プロスタサイクリン,ホスホジエステラーゼ5阻害薬,エンドセリン受容体拮抗薬)の有効例が散見
されるが予後改善効果は不明である1061).心移植でほとんどの例で蛋白漏出性腸症の改善が期待できるが1062),Fontan術後はこれ以外の先天性心
疾患の心移植患者より予後が悪く1063),その至適時期は今後の課題である.
③肺動静脈短絡
肝静脈血流が肺動脈に流入しない術式であるグレンあるいはKawashima手術後に高頻度に肺動静脈短絡が発症し低酸素血症が進行する1064).小
児期にグレン吻合で生じた肺動静脈短絡は肝血流の肺動脈還流を意識したFontan術後には改善するとされる1065).成人Fontan術後患者での頻度は
不明であるが,左相同心ではその頻度は高く,肝静脈血流の不均等に減少した肺に生じることが多い1066).また,高年齢患者では発症頻度は低いとさ
れる.肺動静脈短絡合併例は肺血管抵抗が低く,心拍出量がむしろ増加し中心静脈圧が上昇する場合がある.
治療:小児ではHepatic factorを考慮した肝静脈還流を肺動静に均等に流入させるFontanルートの変更術が有効な場合がある1067).しかし,これ以
外の発症機序も推察されている1068).低酸素血症に対し酸素投与に加え,一酸化窒素吸入の有効例も報告されている1069).また,成人患者で肺血流
とHepatic factorの肺循環流入増加を期待した末梢動静脈瘻作成が試みられ,改善が見られる場合もある1070).
④血栓症
血栓は術後の時期を問わず生じるが1071),経過とともにリスクは増加する1049).抗凝固薬使用の有無にかかわらず発症するが,成人では抗凝固薬非
使用例で血栓関連の心事故が多いとされる1072).Fontan術後患者の止血・凝固因子は異常であることが多く,特にアンチスロンビンⅢ,プロテインCや
Sの低下,第Ⅷ因子増加等の凝固能亢進状態にあるとされる1071).しかし,東洋系(中国人)の凝固系異常は欧米人と異なることが報告され人種差の
存在が示唆されている1073).
治療:血栓予防の有効な抗凝固療法は確立してない.しかし,以下の場合には積極的に抗凝固薬の投与を考慮する.
(1)血栓の存在
(2) 中心静脈圧上昇,低心拍出量,大静脈肺静脈短絡や開窓を有し有意な右左短絡を有する低酸素血症
(3)中等度以上の心室収縮能低下
(4)APCで拡大した右房
(5)Fontanルートの狭窄等の血行動態異常
(6)心房頻拍性不整脈の既往1071)
成人Fontan術後では,肺動脈を含めたFontanルート内の巨大血栓は薬物に加え手術やカテーテルによる除去が必要である場合も多い1074),1075).
血行動態が不安定な場合,その死亡率は75%と高い1072).
⑤心機能低下
体心室収縮性低下,高い後負荷の持続による体心室の仕事効率の低下が,術後遠隔期の心機能破綻に繋がると推察されている1042),1076).体心室
形態も重要な心機能規定要因である.非左室型体心室のQRS幅は左室型体心室に比べ幅広く,内因性の体心室非同期収縮の原因となっている可能
性があり1042),頻拍時や運動時の不利な要因である1042),1043).また,大血管の伸展性低下が示唆され1077),心室の後負荷増大に加え,伸展性低下
による脈圧増大は冠循環低下を生じ,心機能低下の要因となる.さらに,内皮機能低下が運動耐容能低下と関連する347),1078).このため,肺血管
1079)とともに体循環での一酸化窒素に関連した内皮機能維持の重要性が指摘されている.
治療:薬物による抗心不全療法は確立していない.利尿薬は浮腫,腹水や胸水等の不適切な体液貯留には有効である.しかし,成人慢性心不全患
者と同様に,利尿薬使用が死亡の独立危険因子であり注意深く使用することが推奨される1049),1080).レニン・アンジオテンシン・アルドステロン系
(RAAS)を抑制した場合の心臓自律神経や運動耐容能の改善効果は否定的である344),356),1081).β遮断薬の効果は,若年での有用性は散見される
が1082),成人での有効性は不明である.洞機能機能障害を有する割合が高く,徐脈傾向にあり1083),不用意なβ遮断薬使用はむしろ血行動態を悪化さ
せる.したがって,不整脈治療も含めペースメーカ植込みも考慮した循環管理を行う必要がある.房室ブロックでの心室ペーシングや非同期収縮を示す
二腔心を有する体心室では心同期治療を意識した心室ペーシング部位を選択する必要がある1084).
⑥房室弁閉鎖不全
非左室型体心室は,三尖弁や共通房室弁閉鎖不全の頻度が高く,体心室機能低下も同時に進行することが多い.
治療:中等度の房室弁閉鎖不全ではRAAS抑制療法は有効な可能性がある.重度の房室弁閉鎖不全では人工弁手術も考慮した対策が必要であ
る.心機能低下,高年齢や腎機能低下は房室弁閉鎖不全修復時の危険因子であり1085),比較的早期の対策が重要である.僧帽弁以外の房室弁閉
鎖不全の修復は困難で人工弁置換術を考慮する.
⑦腎機能低下
成人先天性心疾患術後は慢性的な血行動態異常が腎機能低下を引き起こすタイプⅡの心腎連関症候群の典型とされている1033),1086).Fontan 術
後もその頻度は高く(17%)1033),心事故との関連が示唆される.低心拍出量や高中心静脈圧はその原因と推察され,手術年齢と負相関することから
1087),術前の低酸素血症による潜在的な腎障害の可能性が指摘されている.
治療:腎機能低下に対する治療法は確立していないが,RAAS抑制療法が有効な可能性がある1088).不整脈発症や心不全時の血行動態管理には
腎機能維持を考慮する必要がある.特にRAAS阻害薬併用例での感染や下痢等による脱水の際は,腎機能悪化に配慮した治療が重要である.
⑧肝機能障害
慢性的な中心静脈圧の上昇は肝鬱血に由来した肝障害を引き起こし,術後経過に伴いその頻度は増加する1034).腹部エコー法やCTは肝硬変検出
に有用で,特にCTが優れている.血液検査からもForns指数[=7.811−3.131・ln(血小板数)+ 0.781・ln(γGTP)+ 3.467・ln(年齢)− 0.014(総コレス
テロール)]は肝硬変検出に有用であるとされ,術後経過期間と高い相関性を示す1034).
治療:肝障害に対する治療介入基準は明確でなく,今後の課題である.
⑨喀血
Fontan術後遠隔期の喀血の報告は散見される.発達した大動脈肺動脈側副血行路が原因とされ,時に致死的な場合があり1035),注意を要する.
治療:胸部CTで出血部位が予測可能な場合もある.大動脈肺動脈側副血行路の有無を検索し,可能であればカテーテルによるコイル塞栓術を行う.
大量出血では輸血が必要な場合がある.
⑩消化管出血
まれな合併症で,原因は不明であるが,蛋白漏出性腸症と関連することが示唆されている1036).
治療:輸血が必要となる場合がある.蛋白漏出性腸症の改善とともに改善する.
⑪大動脈解離
上行大動脈の拡大と大動脈解離を生じた例が報告されている1037).他の先天性心疾患と同様,大動脈壁中膜の弾性線維の構造異常と関連すること
が推察される.冠動脈を含めた大動脈形態評価には造影CTが有用である.
治療:大動脈形成術や置換術が適応となるが,薬物による予防効果は不明である.
⑫耐糖能異常
境界領域を含めた耐糖能異常の頻度は高く(43%),運動耐容能低下と関連する.糖尿病型を示す割合も高く(16%),心事故と関連する1038).高い
中心静脈圧,肝鬱血や利尿薬投与が耐糖能異常と関連するとされている.
治療:食事や運動等の生活習慣改善が推奨される.糖尿病合併例では,内分泌代謝専門医へ紹介することが望ましい.
⑬プラスチック気管支炎
まれな合併症で,小児期の発症がほとんどである.低心機能,高い中心静脈圧や不整脈との関連が示唆されている1039).蟹肉様の気管支鋳型
(cast)が気管支内を占拠し,湿性咳漱や呼吸困難で発症し,致死的な場合もある.
治療:プラスチック気管支鋳型を取り除くことで症状は改善する.気管支鋳型形成予防には,血行動態の改善に加え, ステロイド投与やt-PA(tissue
plasminogen
activator)のエアロゾルが有効な場合がある1039).
外科的治療法
上記合併症のいくつかを伴う, いわゆるFailing Fontanといわれる状態では,右房−肺動脈の直接吻合(APC型) 法からTCPC型の修復に変更する
Fontan conversion法が行われ始めており,一定の成績を上げている396).この手術は,右房バイパス術,右房縫縮術,右房maze手術,ペースメーカワ
イヤー装着等を同時に行う.手術死亡は0~10%,心移植に移行した例は12%,上室性頻拍/心臓細動の再発は,12.5~ 30%で,大部分はNYHA機
能分類Ⅰ~Ⅱと改善している396),1089).
外来管理
遠隔期合併症を意識し,3~ 6 か月ごとの経過観察が必要であるが,患者の病態や重症度に応じた生活の質を意識した生活指導,管理が望まれ
る.また,成人患者は,重症度が高く,合併症のリスクが上昇していることを認識し,患者,その家族と共有することが重要である212).
表83 Fontan型手術術後の主要な遠隔期合併症とその管理,対策

成人先天性心疾患診療ガイドライン(2011年改訂版)
Guidelines for Management of Congenital Heart Diseases in Adults(JCS 2011)
Guidelines for Management of Congenital Heart Diseases in Adults(JCS 2011)